新闻
NEW 药学院尹泰钟教授组利用遗传因子剪刀技术开发出大肠癌治疗剂
- 2020-05-20
- 8374
2020-04-08

我校的尹泰钟教授研究组利用纳米-基因剪刀技术成功开发出了大肠癌治疗剂。这是针对目前广泛使用的大肠癌抗癌剂没有疗效的遗传变异大肠癌患者的治疗方法。
尹泰钟教授(药学系)与加图立大学教授赵英锡(医科大学内科教室)一起,通过在纳米传达体上搭载基因剪刀蛋白质构造体的方式,在基因异常部位上进行了有效的编辑,从而研发出了新的大肠癌治疗剂。相关内容刊登在了著名学术杂志《Nano Research》4月4日的网络版上。论文的题目是《治疗抗癌剂耐药大肠癌的基因编辑纳米粒子系统的治疗性接近(Gene editing particle system as a therapeutic approach for drug-resistant colorectal cancer)。
尹教授组开发的方法是针对目前广泛用于治疗大肠癌的药物具有抵抗性,难以治疗的患者们。"setuximab"抗癌药虽然用于治疗大肠癌,但由于与癌细胞生长相关的KRAS基因变异,很多患者未能达到治疗效果。
大肠癌是因现代人的饮食习惯和生活方式而持续增加的疾病。因此,治疗药物的开发非常活跃,主要使用以抗体为基础的药物。此时使用的药物与EGFR受体结合,抑制癌细胞的生长和生存,从而达到治疗效果。但据悉,大肠癌患者中,60%左右对药物表现出抵抗,不再具有治疗效果。这种情况下,与癌细胞生长有关的KRAS基因变异,相关患者预后非常不好。
许多研究人员正在努力治疗KRAS基因变异导致的癌症,但由于基因变异导致癌症持续复发,他们需要对根本的治疗方法进行研究。因此,虽然一直以利用基因剪刀技术,基因剪刀技术作为替代方案,但由于蛋白质形态的基因剪刀材料在体内的稳定性大幅下降,效率问题很难得到解决。
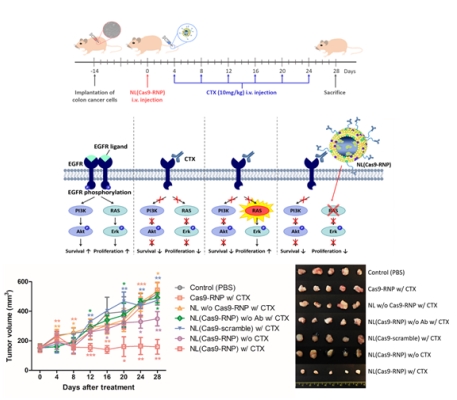
对此,尹泰钟教授研究组在纳米传达体上搭载了基因剪刀蛋白质结构体,通过有效编辑遗传异常部位,取得了较高的治疗效果。研究组使用了纳米脂结构体纳米,搭载了可以编辑 KRAS基因变异部位的基因剪刀蛋白质材料。另外,通过在纳米结构体表面导入用于大肠癌目标的抗体,确认了基因剪刀材料的稳定性和治疗效果最大化.从活体内的实验(in vivo)向癌组织传递基因剪刀材料的效率达到60%,在动物模型上的治疗效果与对照群相比显示出了较高的治疗效果。
尹泰钟教授表示:"现有的基因形态的基因剪刀材料是利用病毒传达体,适用于生物体的结构,传递效率低,而且会编辑到自己不愿意看到的地方,其副作用(off-target效果)是个问题。""作为替代方案,由蛋白质结构体构成的遗传因子的剪刀材料浮出了水面,但在注入生物体内后,随着酶的分解,传递,编辑效率降低,因此一直存在局限性。"
对此,尹教授的研究组发掘出了可以活体使用的材料组成的纳米构造体。基因剪,利用基因 上的问题,编辑从根本上治疗的可能性就越高,体内注入稳定性有所下滑的问题,克服了。
尹教授表示:"现在为了治疗癌症,在试管环境(in vitro)中使用了能够调节免疫细胞活性的基因剪刀技术","期待今后通过直接在体内注射,将治疗效果最大化"。
KRAS基因变异导致的癌症不仅与大肠癌有关,还与胰腺癌,肺癌,卵巢癌等许多癌症疾病有关,为克服难以治疗的癌症疾病,需要纳米-基因剪刀技术。
尹泰钟教授在过去20多年里一直研究纳米材料,能够有效地将多种生物物质传递给细胞或组织。近年来,由于基因剪刀技术的局限,为克服体内稳定性和细胞渗透率,口服无法治疗等问题,科学家一直集中精力研究采用纳米技术。尹教授担任我校产学合作团下属的npoyu技术控股公司(株)mojin medi的代表,计划通过该公司进行临床实验。
(注:本文出现的所有人名均系音译)
